注册登录才能更好的浏览或提问。
您需要 登录 才可以下载或查看,没有账号?立即注册
×
ISO 17511发表于2003年8月15日,时间过去了8年。很多专家非常乐观,认为: …将会制备出越来越多的(有证)参考物质…,解决临床实验室检测结果的溯源性。但是,认真回顾这8年内,国际上有多少新的参考物质或参考方法被批准认可了?新发布的ERM-DA470参考物质,替代原先的CRM 470。似乎至今都对发布的ERM-DA470k众口称赞,认为是实现溯源性又一个范例。可是,却没有去深入研究,由此又引出了什么值得我们令人深思的问题?
以下,我对近期来与蛋白关联的标准化问题作介绍。
一、JCTLM确定了特定蛋白免疫参考方法
在免疫检测参考系列上,经常在争论:哪个检测方法是最好的?很长时间内,临床实验室总是被误解认为:免疫散射比浊最好,而且它就是特定蛋白检测的参考方法。其实在上世纪的1990年代中,从建立CRM 470参考物质起,国际上早就将免疫单向扩散、免疫散射比浊、和免疫透射比浊三个技术,一起用于为CRM 470内的14种蛋白进行值的设定。
以后,国际上在建立载脂蛋白A和B的标准化物质中,依然采用了这三个免疫方法为这两个分析物的参考制品定值。实践反复说明了:这三个方法在检测分析性能上具有的水平等当。
2008年6月13日,国际检验医学溯源性联合委员会(JCTLM),已经发布公告,宣布粒子增强的免疫透射比浊、和粒子增强的免疫散射比浊均为JCTLM认可的参考程序。2010年在介绍胱蛋白酶抑制剂C的标准化参考物质ERM-DA471文章中,专门提到了:使用了几个免疫检测程序进行了特性检测(不同的分析原理为:颗粒增强免疫透射比浊、颗粒增强免疫散射比浊、和酶放大的单向免疫扩散)和多个不同的抗胱蛋白酶抑制剂C抗体进行检测。
这些程序的原理近期已经被检验医学溯源性联合委员会(JCTLM)列为参考方法。
因此,我们不要再为免疫透射比浊和免疫散射比浊这两个技术去争论高低了。它们都必须是使用粒子增强后,才被认可为检测蛋白的参考程序。
二、认识ERM-DA471:胱蛋白酶抑制剂C的标准化
1、首先要解释的是,原先欧洲标准参考物质均以CRM命名,这个CRM(Certified Reference Material)是有证的参考物质之意,没有特别指出是欧洲的参考物质。现在改为ERM(European Reference Material)正式表明是欧洲的参考物质。DA之意是欧共体的参考物质和参考测量研究院(IRMM)在分类各种参考物质时指出该物质性质的分类性质代码。D:在组成中被证实的与健康关联的基质物质;A:D类中为人的体液(人体体液:血清、尿液等)。后面的471只是各个参考物质的序号而已。
2、ERM-DA471:2010年5月,欧盟联合研究中心委员会(European Commission Joint Reaserch Center,JRC)发布了胱蛋白酶抑制剂C(Cys C)的参考物质ERM-DA471。该参考物质的证书说证实了该参考物质内CysC含量为5.48 mg/L,不确定度为0.15 mg/L。并说明:1)在复溶物质中Cys C,由粒子增强的免疫散射比浊、粒子增强的免疫透射比浊、和单向免疫扩散三个检测方法进行检测。2)该定值由4个实验室各自检测,由7个可接受均值的未加权均值确定。证实的质量浓度,通过Cys C的纯蛋白制品可溯源至SI单位。3)扩展因子k=2的综合不确定度U,相当于95%的可信水平。这是按照GUM,ISO,1995导则估计的。特别须注意的是,该参考物质在出售后一年有效(此点与原CRM470宣布的有效期可长达10年绝然不同);注明了最小用量为2μl。
三、 CRM 470 的推出对全球多个蛋白检测质量的影响
1989年国际临床化学和检验医学协会(IFCC)成立血浆蛋白委员会和IFCC科学部一起,研究和实施对人血清蛋白的含有基质的参考物质的处理、确认、和定值。1993年,共同体的参考局发布了CRM 470(以后被重新评价和命名为ERM-DA470),被确认为14种蛋白的参考物质。
由于CRM 470已经为多个特定蛋白的标准化服务了近20年。确实使这些项目的检测结果在全世界范围内的可比性有了实在的进步。
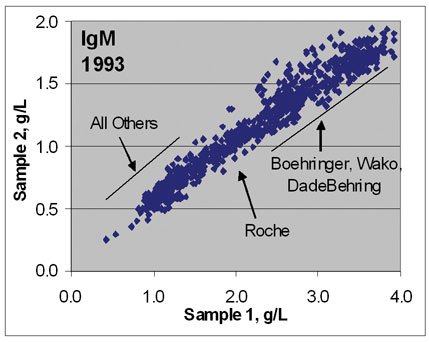 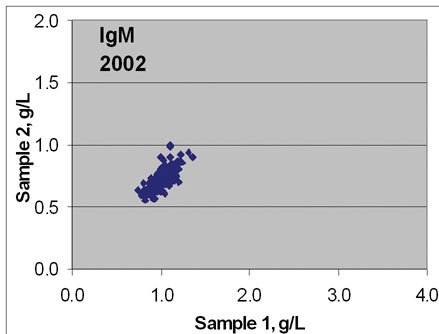
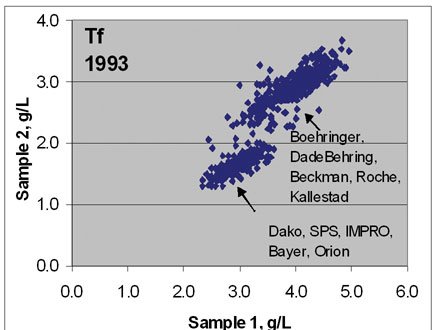 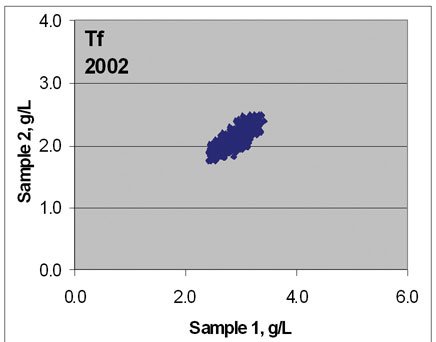
图1 欧洲室间质量评估(DGKL EQAS)结果,显示了各个公司使用CRM 470为他们产品的参考物质前后(1993年和2002年)质量调查结果有了明显的改善。图上部分为免疫球蛋白M(IgM),下部分为转铁蛋白(Tf)。
图1经常被来自欧洲的学者展示,说明CRM470确实为改善14种特定蛋白的检验质量起了重要作用。可是,近期在网页上搜索到的其他类似室间质量比较的资料时,我震惊了。图2同样为DGKL的EQAS比较图,是C反应蛋白的。图示清楚反映了有了CRM 470的以后,CRP检测质量似乎更差了。为什么以前就看不到呢?这不是偶然的。能看到这个图的时间,也就是现在推出专为CRP服务的参考物质ERM-DA472的时间。Thomas B等在2001年就报告了:血清蛋白值的互换性:美国生产厂商使用CRM 470设定值依然在厂商间有偏倚。他们指出:在引入国际参考物质(CRM 470;人血清蛋白参考制品〔Reference Preparation for Proteins in Human Serum〕)的7年后,血清蛋白值在厂商间依然有显著差异。有些蛋白如前白蛋白和C4,它们的偏倚事实上还在增加。所以,他们建议为了改善实验室间结果的互换性、以及若要形成一致的参考区间,需要对标准化作进一步的努力。问题变得更清楚了,CRM 470的使用确实为全球的14种蛋白的日常检测水平有了改善,但是,也许在科学家认为的CRM 470的稳定期内,某些蛋白变得不稳定了;有的内含蛋白本身就很复杂,随着检验技术的发展,它们在先进的检验技术中表现得不一致了?总之,检测结果的互换性有问题了。
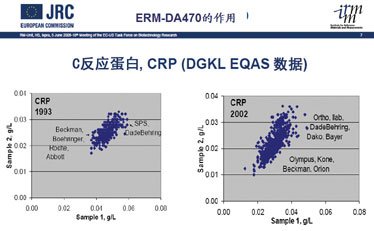
图2 欧洲室间质量评估(DGKL EQAS)结果,显示了各个公司使用CRM 470为他们产品的参考物质前后(1993年和2002年)CRM质量调查结果并未如预期那样有改善。
今年刚发表在Clin Chem Lab Med第8期杂志上,代表国际临床化学学会(IFCC)的血浆蛋白委员会(C-PP)发表了“全球标准化血浆蛋白检测‘一个挑战的计划’”重要文章。在参考物质ERM-DA470k/IFCC的可用性对血清蛋白一致性的作用中,专家们认为:在1990年代前实验室间和厂商间在血清蛋白检测得到的值变异过大,是推动形成CRM470的主要动力。在发布了CRM470后,不少国家的室间质量评估计划的调查结果[包括来自UK(UK NEQAS)、瑞典(EQAS)、德国(DKGC-RfS)、捷克共和国的、和美国(CAP)]说明: AAT(抗胰蛋白酶)、HPT(结合珠蛋白)、和TR(转铁蛋白)的实验室间结果有了真实的一致性,C3、C4和免疫球蛋白有了中等程度的一致性。与AAG(α1-酸性糖蛋白)和TTR(白蛋白)的结果不同,CER(铜蓝蛋白)的变异基本上没有改变。CRP的资料在以往的所有发表资料中均未包括在内。但是,CRP检测,经典的和“高敏”的二者,均显示了实验室间和厂商间的变异,2000年代较CRM470发布前有了更高的变异,可能因厂商忙于引入高敏检测。
近期QA计划已经显示了,总体上所有蛋白的实验室间变异没有进一步的下降,有些还有增加。美国和英国以往发表的结果,修改后包括在2009数据中,参见图3。英国QA显示了实验室间的CV,而美国为检测间、或“厂商”间的CV(有些厂商有多个检测系统)。来自各个实验室的数据在美国数据中是没有的。由C-PP以往的报告,以及这个报告,浓度非常低的蛋白均未包括在内。正如看到的,多个蛋白的CAP调查的厂商检测变异依然很大,在德国QA中也如此。涉及多个因素,包括从ERM-DA470转换给厂商的一级校准品的是不最合适的值,随后传递给了产品校准品和控制品。很差的校准曲线拟合和使用不稳定的校准和控制物质等也为此有影响。
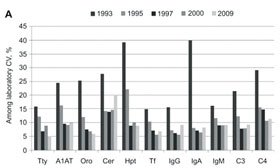
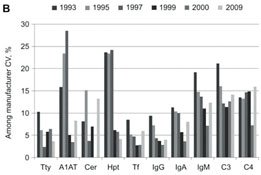
图3 A为英国(UK NEQAS)蛋白检测的室间质量评价计划,实验室间CV的平均CV。B为美国CAP的厂商间CV的平均CV。
Tty为白蛋白、A1AT为α1-抗胰蛋白酶、Oro为α1-酸性糖蛋白、Cer为铜蓝蛋白、Hpt为结合珠蛋白、Tf为转铁蛋白。
如果蛋白浓度非常低时、如果检测用抗体在识别的决定簇有显著差异时、或这些的综合,几乎所有常用的检测方法依然有问题。例如,CER是一个非常异变的蛋白,若该蛋白不是完整无缺的,不同的抗血清会与不同的片段反应。正如上述说明的,对这个蛋白检测的一致性基本上在所有报告中很少有最佳的。补体C4像CER和TTR(前白蛋白)那样,在健康个体中的浓度相对较低,是对常规(非增强的)的免疫检测是一个挑战。生理学上,大多个体的CRP浓度低于2 mg/L,对这个浓度的检测,要求增强灵敏度(如包括:粒子增强的散射比浊或透射比浊、酶或荧光的免疫检测)。即使使用了这些检测方法,CRP的一致性依然很差。图4为Youden图,是2009年CAP发出两个标本进行CRP调查,报告的中位数的中位数分别为1.2 mg/L和2.9 mg/L。可看到值的离散超出8倍范围。2009年德国的CRP调查(DKGC-RfS IG4/09)结果见图5;本次调查的中位数浓度较CAP样品高15倍,但即使这样高的浓度可注意到明显的变异。
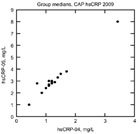
图4 2009年CAP的CRP调查。每点代表使用相同检测系统(相同方法、相同平台、相同校准品)的所有实验室结果的中位数。

图5 2009年德国(DGKL-RfB)对CRP调查的Youden图。IgG4/09代表的是样品代码,不是被分析物。离群点没有在图中。
图6为2009年英国的UK NEQAS对CER调查结果Youden图。结果也显示了被报告浓度很宽的范围,虽然在比例上的差异(即一个样品与另一个样品的值的比率)较CRP要少一些。

图6 2009年UK NEQAS的铜蓝蛋白调查。各个实验室一对结果的Youden图。
很明显,引入CRM-DA470对多个血清代表的厂商间和实验室间的变异有了真实的下降,包括AAT、HPT、TRF、三个主要的免疫球蛋白、和补体组分。但是,近期的数据说明,与1990年代的后期比较,变异还略有增加;TTR、CER、C4、和CRP继续显示了厂商间差异的增大。
四、ERM-DA470k/IFCC和ERM-DA472/IFCC取代CRM 470
由于本世纪初期CRM 470即将用完,需要完全按照原先制备CRM470的工艺,重新制备新的一批参考物质,也应被命名为ERM-DA470。可是,尽管在收集原材料(人混合血清)、加工处理、添加各种物质、分装和冻干等等步骤完全重复了1992年当时制备CRM 470的步骤,甚至连加工处理的地点也依然在原德国的Boehringer。可是,现在却用两个ERM-DA470k和ERM-DA472参考物质替代原CRM 470,这又是为什么?
在加工预试验中,发现了CRP经冷冻干燥后,ERM-DA470(原CRM 470)参考物质的冷冻干燥和复溶后,对CRP回收不佳,对CRP蛋白使用了两个市售方法在多个实验室做了检测(见图7)。原因是冷冻干燥处理使CRP产生了自身凝聚,形成众多不一致的低聚物。这样,参考物质内的CRP不能如天然样品内的CRP,自由地参与免疫反应。冷冻干燥物质内CRP瓶间的非均相性高;存在不同的低聚物。使用这样的参考物质进行校准的过程会因低聚物状态多变而变化,由于检测的技术原因,将中止溯源性链。
为了提供一个对CRP最佳的条件,将按照原制备CRM 470形成的液体物质,在进行冻干前,分出一半分装后进行液体冰冻保存,成为CRP专用的参考物质ERM-DA472/IFCC。 另外一半分装后依然冷冻干燥处理,形成其他蛋白的参考物质。为了与过去的参考物质有所区别,该参考物质被命名为ERM-DA470k/IFCC。需要特别说明的是,在原CRM470制备和定值过程中,却没有发现因冷冻干燥是CRP自身聚合导致结果偏低的表现。
似乎所有都非常合理,就是因为发现了CRP不可冷冻干燥,所以才成为今天的两个参考物质。对它们的定值也采用了原ERM-DA470为参考,以过去为ERM-DA470定值的方案,在多个参考实验室协同定值。因此,该两个新参考物质的定值可以溯源至原ERM-DA470(CRM 470)。所以,对目前这些分析物(被测量)的可靠性依然保留了原先的溯源性。
为了弄清楚以往CRP标准物质是否也一直被冷冻干燥予以保存,我查阅了文献。结果发现,在1992年前为原ERM-DA470定值用的人CRP的第一个国际标准,代码为WHO 85/506。一个安瓿的人CRP Code 85/506内含有0.049 IU,或含有49 mg CRP。该物质也是冻干品。
发现CRP不能被冻干的时间为2007年,可是为该深低温保存的CRP参考物质定值用的是原ERM-DA470(原CRM 470),它是冻干的。为ERM-DA470定值的标准参考物质是WHO 85/806也是冻干品。
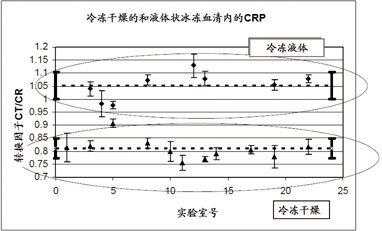
图7 冷冻干燥处理后CRP的检测结果仅为未经冷冻干燥深低温保存的CRP检测结果的80%。
冻干会使参考物质制品内的CRP形成非均相的低聚物,使其参与免疫反应能力逐渐下降。我的问题是:用一个至今还没有完全证实在原CRM470中是否CRP已经出问题的情况下,以原CRM 470去为新的ERM-DA472定值,尽管在溯源性上思路很清楚,但是,这个定值正确吗?而且,当初为原CRM 470的CRP定值时,用的是冻干的WHO 85/506,也许可以这样估计,从原先的CRM 470开始定值起,就已经是问题了;随着时间的推移,再拿这个原CRM 470为ERM-DA472定值时,相隔了十多年后,在参考物质上标示的值没有变,可是,如果能让上世纪90年代刚做出来的CRM 470不再变化的话,那么与2007年为ERM-DA472定值时的那个CRM 470相比,可以说十多年前的内含CRP可参与免疫反应能力的要比最近使用的那个参考物质内的CRP要强;即内含“CRP”在下降,但标示值不变;使病人样品检测的CRP结果在随着CRM 470使用时间的推移在逐渐“升高”。这样的溯源性有多少意义?
从今天的认识来说,20余年前的科学家还没有知道冻干对CRP值的影响,不懂者无罪!但是今天已经知道冻干对CRP的影响后,还依然使用明明知道是不对的参考物质为已经纠正的新参考物质定值。溯源性是有了,但是正确度何在?究竟追求溯源性的目的是什么?
我突然悟出一个道理。在ISO 17511的引言中说:为了使检验医学量的测量得到正确的医学应用、不论在何时何地都具有可比性,量值必须有明确的定义、报告给医生或其他卫生人员及患者的结果必须准确(正确和精密)。临床实验室的所有测量结果要得到正确的临床应用,这是实现溯源性的第一个原则。恰好就在从1990年代起到本世纪的近20年,临床医学使用高敏CRP对于心血管疾病的急性发作的预示作用价值被真正地确认了。闻名的全球JUPITER临床试验充分地肯定了:凡是高敏CRP检测值≥ 3 mg/L的表面健康人群,在未来的10年里发生心血管疾病问题的可能性是高敏CRP≤1 mg/L的人群的3倍以上。不仅如此,还发现了服用他汀类药物可以使CRP值下降,随之发生心血管疾病的发病率也随之下降。这是近20年来在检验医学上得到的重大成果。而恰恰这时候,出现了CRP结果可能不正确的问题。是要全面否认几十年的临床成果、还是保留现状,继续认可结果的可靠性;这是一个重大抉择。正因为如此,我仅从旁侧估计,也许这就是依然坚持CRP的病人检测结果可靠性和溯源性主要原因。
难道现在还拿不出更好的CRP标准物质和为二级参考物质定值的参考程序?不是!
美国的国家标准和检测研究院(NIST)化学科学和技术实验室Bunk博士,已经研究成功全新的CRP参考测量系统。
测量步骤:
1、以核素标记的rCRP加于样品中;
2、以单克隆抗体纯化添加过CRP的样品;
3、以胰蛋白酶消化添加过CRP的样品,分离CRP;
4、以MRM-为基础的核素稀释LC-MS,对多个CRP胰蛋白酶消化的多肽量化,使用标记的和未标记的CRP制备的校准品(即:双核素稀释质谱分析)。具体步骤如图8所示。
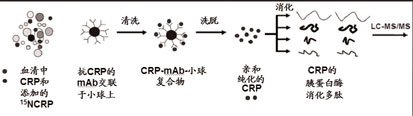
图8 新的CRP参考测量系统
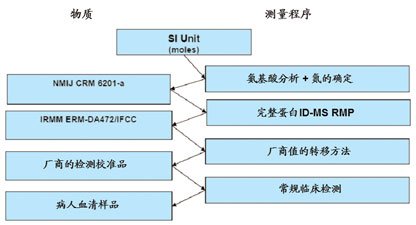
图9 理想的CRP溯源过程
按照上述NIST的CRP参考测量系统,可以对NMIJ CRP 6201-a正确定值,并在以后的溯源途径中,将可靠性传递给病人样品的检测结果。
还有一个重要问题是,原CRM 470内有14个特定蛋白被定值。现在的ERM-DA470k却只有12个特定蛋白的定值了。14减1应是13,怎么又少了一个呢?原来的14个特定蛋白为:α1-酸性糖蛋白(A1AG)、α1-抗胰蛋白酶(A1AT)、α2-巨球蛋白(A2M)、白蛋白(ALB)、补体C3c(C3c)、补体C4(C4)、铜蓝蛋白(CER)、C-反应蛋白(CRP)、结合珠蛋白(HPT)、免疫球蛋白A(IgA)、免疫球蛋白G(IgG)、免疫球蛋白M(IgM)、转铁蛋白(TF)、前白蛋白(TTR)。仔细核对,现在的ERM-DA470k中,除了CRP外,还少了铜蓝蛋白(CER)。在候选的参考物质和它们对参考物质互换性中,因在候选参考物质中的铜蓝蛋白存在了非典型异构体导致了阴性影响。在为ERM-DA470k/IFCC确定特性时,相对于ERM-DA470/IFCC校准时,有两组常规方法,它们的结果差异约10%。在这两组常规方法间有着相同大小和方向的差异,在EQAS计划中也观察到该差异。这个非典型异构体可被两组最佳常规方法检出有显著差异。(见图10)
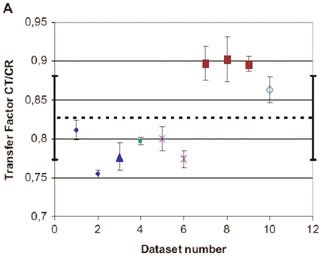
图10 ERM-DA470k中的铜蓝蛋白被两个检测方法检测的结果间差异的表现(图左下侧为一个方法检测的表现,图右上侧为另一个方法检测的表现)。
CRM 470中的铜蓝蛋白看来更多地像天然的血清样品。非典型异构体组分的多少会影响检测结果。在CRM 470中,没有被充分地予以确定特性,导致至少有一组常规方法引入了未被控制的校准偏倚。为此,CRM 470不适合作为校准品为ERM-DA470k/IFCC内的CER定值,在ERM-DA470k/IFCC中,至今未对该蛋白予以确认。正在进行的研究期望解决这个问题。
五、肌钙蛋白I
由于心肌梗死诊断的紧要和迫切性,使用肌钙蛋白对疑似心肌梗死病人的检测是当今的主要项目。因为肌钙蛋白T(cTnT)被Roche(原Bergmeyer)公司专利垄断,其他公司只能开发肌钙蛋白I(cTnI)项目。可是,尽管各个cTnI产品均被批准可用于临床,但是,各个公司的cTnI产品对病人样品检测结果间,结果无可比性,差异可达百倍!自上世纪以来,一直认为,国际上缺少肌钙蛋白参考物质,才是可比性差的主要关键。经过多年的研究,美国国家标准和技术研究院(NIST)于2006年发布了人心肌肌钙蛋白复合物标准参考物质(SRM)2921。临床实验室和医学界都普遍认为,以后所有cTnI均采用SRM 2921为一级标准,校准它们的cTnI产品,可以使cTnI对病人的检测结果可比性有很大的改善。可是,临床应用的结果显示了:该参考物质与病人血清的互换性较差,用于不用SRM 2921得到的病人结果的离散程序并未变化。但是,干脆使用一个混合血清,以某个检测系统为其定值,然后,所有其他公司的cTnI检测结果,均以该血清的定值进行临时校准后,再检测其他血清,发现现场方法的检测cTnI间的变异范围:使用SRM 2921直接校准的为82%~97%,中位数为88%。使用混合血清协同校准后,混合血清的cTnI方法变异减少为9.0%~23%,中位数为15.5%。 使用混合血清的简单做法,可改善现有方法的协同5倍以上。
是什么原因使cTnI的病人血清结果比对这样差?从NIST的资料中,可以清楚地知道,原来cTnI更加是一组蛋白的组合。图11为使用液相层析质谱分析人心肌内cTnI的各个蛋白相对分子质量分布情况。
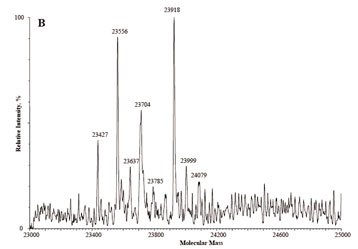
图11 使用液相层析质谱分析人心肌内cTnI的各个蛋白相对分子质量分布情况。
图中的每一个分离的小峰都代表的一个不同相对分子质量的cTnI。在这个cTnI的大家庭内有如此多的“成员”,难怪不同公司在提取认为符合要求的cTnI的蛋白时,实际上是不同cTnI的蛋白或其组分的组合,由此免疫产生的抗体形成的试剂盒,当然会得到完全不同的检测结果。著名的Mauro Panteghini认为,在血液中,存在的cTnI是一个具有不同分子类型的非均相混合物,因为其非均相性引出了现在的分析问题。若能识别混合物的所有组分中共有的、分子的一致的不变部分,并由此用于形成cTnI检测的抗体,可选择性地识别这个不变异部分内的决定簇,才可导致免疫检测反应性均一性随之而来的增加。
还有,在心肌损害将肌钙蛋白释放到血液时,肌钙蛋白很容易被氧化、磷酸化、甚至C-端被切断、出现被转换后的修饰类型等。所以,如何识别一个未被修饰过的真正cTnI分子是检测可靠性的关键。
因此,要使cTnI检测标准化,不仅需要一个国际认可的参考物质(如SRM 2921),从经验告诉我们,不可能直接使用公认的参考物质可以使检测结果具有可比性;如果在现有的各个公司试剂盒中筛选出较理想的一对单克隆抗体,经验证后,要求所有公司都使用相同的单克隆抗体形成它们的试剂盒;加上公认的参考物质,建立一个如ERM-DA470k那样的以血清基质为基础的二级参考物质;以后,所有公司就可以直接使用这个二级参考物质对各自的cTnI产品校准,相信结果的可比性会得到实现。2010年的IFCC肌钙蛋白I标准化工作组发表文章:肌钙蛋白I候选二级参考程序(较高计量等级免疫检测方法):1.抗体特性和初步的确认(Development of a candidate secondary reference procedure (immunoassay based measurement procedure of higher metrological order) for cardiac troponin I: I. Antibody characterization and preliminary validation)。报道了研究形成了二级检测程序(方法)(RMP)以支持促进肌钙蛋白I(cTnI)标准化。RMP应用于对血清为基础的二级参考物质定值,这些血清没有人为添加物引入的偏倚。使用彩色微球技术和十二硫酸钠聚丙烯胺凝胶电泳(SDS-PAGE)证实RMP的最佳单克隆抗体对。使用这些抗体形成ELISA方法,准确地检测存在于血清的主要cTnI形式。建议的RMP看来在检测含有各种类型肌钙蛋白复合物、磷酸化的和去磷酸化的形式、和存在肝素时,均没有出现偏倚。候选方法对于检测建议的cTnI二级RM时,具有合适的线性和灵敏度。初步使用血清与商品的cTnI试剂盒比对,也支持了以RMP对RM定值的适用性。对RMP的整个确认和最后的评估将通过互换性和相互比较再作评估。这些实验结果说明上述的设想正在逐步实现。
六、特定蛋白标准化遇到了问题
1、分析物究竟是什么?
随着人们对临床关注的这些蛋白生物标志物深入研究,较之以往有了非常大的进步。几乎所有这些蛋白的每一个,都简直是一个大家族!不对蛋白的每个家族有完全深入的了解,是无法实现标准化的。
另外,进行参考物质和参考方法研究的上层科学家,如果只从参考层次上去建立参考系列,而不考虑常规检验的方法具有的情况,要实现溯源性或正确度的传递都是空话!
蛋白的生物标志物,其项目或被称为“分析物”的对象,并不是以往想象的单一分子结构(如无机盐氯化钠)。它们在样品中存在的状态,因被解离、修饰(糖基化、氧化、脱酰胺、磷酸化等)、二级和三级结构、多聚体表现、凝聚程度等,使各个被检测的蛋白生物标志物实际上是具有“相同”名称的许多类似结构分子复合体。
因此,不同厂商使用的抗体对于抗原决定簇专一性不同,相同样品的检测结果就会不同。
可以认识的结论是:被测量的定义不明确。是使检测结果缺少可比性的根本原因。
2、溯源性与“共产主义”
随着深入学习,我个人将临床实验室实现溯源性的追求比作共产党人追求共产主义。
马克思发表“共产党宣言”时,他没有看到资本主义以后的发展。在百余年的斗争和实践中,才知道共产主义是一个远大远大远大的目标!
实现临床实验室对病人检测结果的溯源性,正是希望超越时间和空间,不论在何时和何地,病人样品的检测结果在全球具有可比性。
现在看来,溯源性标准化的路漫漫!2003年至今被认可的参考物质和方法仅HbA1c最有代表性。“路漫漫其修远兮,吾将上下而求索”这句出自屈原的名作《离骚》,我们应该很熟悉了。意思是说:在追寻真理(真知)方面,前方的道路还很漫长,但我将百折不挠,不遗余力地(上天下地)去追求和探索。
更多的分析专家越来原重视常规实验室的常规方法。因为,大量的实验告诉我们:实现溯源性的最终,是在临床第一线的检验科。忘记了检验科,何来溯源性!目前,在参考标准化的研究上,较前10年有了很大的进展,要更讲究实际。但是,不论如何:始终使用病人标本作为实验的对象,始终进行方法学比较作为判断是否实现溯源性的依据。现在,更被大家认可!
七、较之量值溯源,当前更应关注的是量值等当
检验界一直在追求实现一个理想的梦:一个病人样品走遍世界,在任何一个临床实验室对样品的检测结果相互具有可比性。
溯源性也正是为此提出的。在近十年前,当时的认识认为:只要为所有的检测项目建立国际上认可的参考物质或参考方法,通过体外诊断厂商实现量值的溯源,临床实验室使用这样的检测系统的产品,世界大同就会实现!
可惜,现在看来不简单!
在开始认识溯源性的时候,我当时就认识到:实现各个临床实验室间检测结果的可比性,还是首要的。不论有些项目还无法表示出溯源性,但是追求可比性在任何时候都是最重要的。
所以,一个县市、一个地区如果能在可比性上下功夫,比论述有多少项目实现溯源性更重要。
最牛的公司可以明确叙述它的系列产品,有许多都实现了溯源性。但是,仔细查阅可以发现:
1、溯源性的源头不是被测量。如HDL-C的溯源性是胆固醇标准加CDC的超离心的参考方法。我怎么知道,被检测的真的是HDL-C?其实,当今的直接方法检测HDL-C和LDL-C,没有一个可以对有病的样品作出可靠结果!
2、坚持说有溯源性(有溯源表格),可是拿不出任何证据可以具体说明确实是如何实现溯源的。这是最多的。
3、自己仅有试剂盒,去买了如罗氏校准品,配合一起提供。宣传说:因为罗氏校准品有溯源性,所以,你也可以实现溯源性!
4、一个试剂盒、一个校准品(仅一个校准值)。公司说任何仪器都可以用,都实现了溯源性。均属虚假行为!
由于中国市场的巨大、微妙、复杂;民营、官方、团体、个人行为交叉,监督部门还不懂装懂,所以,只讲溯源性,似乎老百姓的化验就好了。
说到底,无论“互认”、“可比性”是一回事。
必须认真考虑如何实现可比性,也即:量值的等当。
正当我在溯源性问题上感到迷惑时,突然看到刊登在2008年CCLM上的一篇文章:局部回归:检测系统比较分析的新方法。作者提出,按照预先确定的与水平关联的可接受限值,这个方式可提供两个检测系统间计量上等值(metrological equivalence)的证据。令我大开眼界。Equivalence该词语的中文解释为:(数量、力量、意义、重要性等的)相等;等价;等效。在临床实验室检测一个病人样品某分析物时得到的结果,若能与其他实验室得到的结果在某个允许误差限值之内等值,我们就认为这两个实验室间的结果是可比的。其实,Equivalence在临床实验室的真实含义,我还是认为理解为等当或等值更好。
“等当”一词今天出现在老外的文献中,可谓是最佳的使用。“等当”不是在数量的完全相等,它很真实地描述了现今各个实验室检验结果良好状态。等当就是互相间差不多。不去纠缠有无实现了溯源性,我们相互间同一个样品的相同项目的检测结果很相近,行政领导也认可了。
即使一个实验室的某些项目使用了真的具有溯源性的产品进行检测。如果在这个医院内,还有多个临床实验室的部门。为了使各个部门的结果有可比性,使用病人样品进行比对,实现了可比性。可是,仅那个使用了具有溯源性产品的那个实验室部门有溯源性,其他部门尽管有了可比性,但是,不能说明也具有溯源性。因为,在各部门间的样品比对成功,不说明实现溯源性(平级间的比对,不是向高一级实验室参考方法的比对)!
在ISO 17511标准中明确指出:如上的比对不具有溯源性,---在相同的计量水平下,测量相同量的两个测量程序的测量结果具相关性,但是这样的“水平”相关不提供计量可追溯性。
无独有偶,今年8月美国临床化学协会(AACC)刊登了一篇重要文章:临床实验室检测程序一致性的途径。文章系统地阐述了当今临床实验室应该更多地关注如何使目前还只是有二级参考物质的、但没有任何参考程序(方法)的被测量,以及既无参考物质又无参考程序的被测量,使这两类检测项目的检测系统对病人样品结果具有一致性。实现一致性(Harmonization)的衡量指标就是在方法学比对中使比对结果的量值等当。
|